
大問1
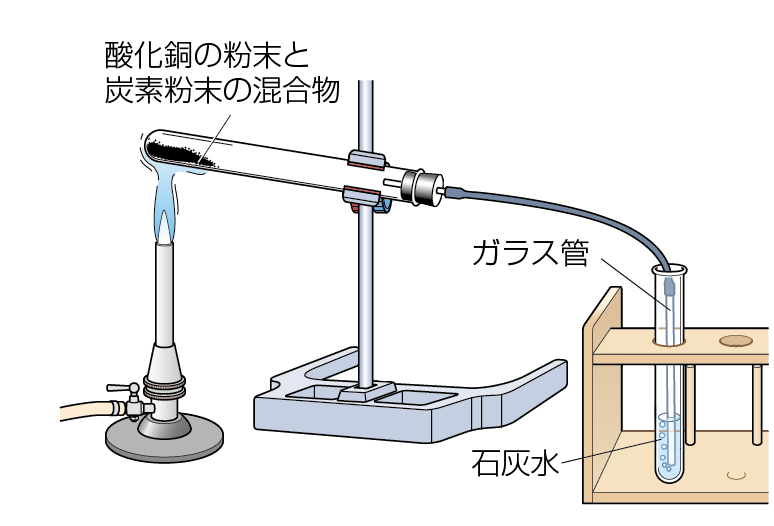
酸化銅の粉末と炭素粉末をよく混ぜた混合物を図のような装置で加熱すると,気体が発生しました。
□① 加熱後,試験管に残った物質は,どのような色をしていますか。また,この物質の名前と化学式は何ですか。( 赤色,銅,Cu )
□② 石灰水の色はどのようになりますか。また,その理由は何ですか。( 白くにごる。 )( 二酸化炭素が発生したため。 )
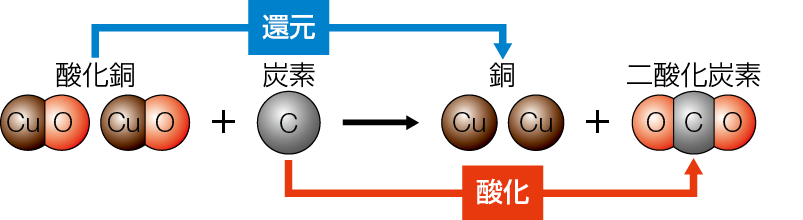
□③ この実験で起こる化学変化を化学反応式で表しましょう。( 2CuO + C → 2Cu + CO2 )
□④ この実験で,還元された物質は何ですか。( 酸化銅 )
□⑤ この実験で,酸化された物質は何ですか。( 炭素 )

大問2
寒いときに使う使い捨てカイロの包装を見ると,その成分は,鉄粉,水,活性炭,食塩などと表示されていました。
□① カイロが包装に入っているときには,もんだり,ふったりしても温かくなりません。それはどうしてですか。 ( カイロの鉄粉が空気と接していないため,鉄の酸化が起こらないから。 )
□② カイロを包装から出して使用しているうちに,温かさを感じなくなりました。これはなぜですか。( 鉄がそれ以上酸化しなくなり,熱が発生しなくなったため。 )


▶酸素に注目したときの化学変化(p.59〜65)
□酸化物から酸素がうばわれる化学変化を還元という。還元は,酸化と反対の化学変化である。還元が起こるときは,同時に酸化も起こっている。

▶化学変化と熱(p.66〜68)
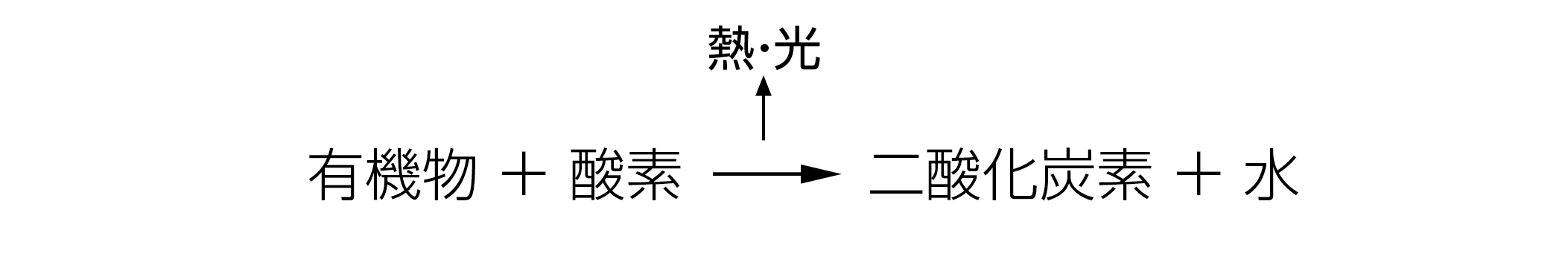
□有機物を燃やすと,熱が発生し,二酸化炭素と水ができる。
□化学変化のとき,温度が上がる反応を発熱反応という。温度が上がるのは,化学変化にともなって熱を外部に放出するからである。また,温度が下がる反応を吸熱反応という。温度が下がるのは,化学変化をするために熱を必要とし,外部から熱を吸収するからである。